Biobran / MGN-3, арабиноксилан из рисовых отрубей, увеличивает активность NK-клеток у престарелых испытуемых: рандомизированное, двойное слепое, плацебо-контролируемое клиническое испытание
AHMED F. ELSAID, MAGDA SHAHEEN and MAMDOOH GHONEUM
Ахмед Ф. Эльсаид, Отделение общественной медицины и общественного здравоохранения, медицинский факультет, Университет г. Эз- Загазиг, Эз-Загазиг, 44519 Аль-Шаркия, Египет;
Магда Шэниин, Отделение Внутренней Медицины, Университет медицины и науки им. Чарльза р. Дрю, Лос-Анджелес, Калифорния 90059, США
Мамду Гонеум GHONEUM, Отделение Хирургии, Университет медицины и науки им. Чарльза р. Дрю, Лос-Анджелес, Калифорния 90059, США
Получено 11 Июня 2016; Принято 28 Ноября 2017
DOI: 10.3892 / etm.2018.5713
Краткий обзор
Старение связано со снижением функции натуральных киллеров (NK) и натуральных Т-киллеров (NKT), что может способствовать повышению восприимчивости организма к инфекциям и риска развития злокачественных новообразований. Проведено предварительное исследование гипотезы о том, что денатурированная гемицеллюлоза с известной иммуномодулирующей активностью – арабиноксилан из рисовых отрубей (Биобран/MGN-3) – может противодействовать снижению активности клеток NK/NKT в гериатрии. В общей сложности 12 здоровых гериатрических пациентов обоего пола старше 56 лет приняли участие в рандомизированном, двойном слепом, плацебо-контролируемом клиническом исследовании. В общей сложности шесть человек служили контролем, а шесть человек принимали Биобран / MGN-3 (500 мг / сут) в течение 30 дней. Влияние добавки Биобран/MGN-3 на активность NK/NKT клеток оценивали с помощью метода дегрануляции. Все испытуемые контролировались на предмет развития нежелательных побочных эффектов. Кроме того, оценивали фармакологическое действие Биобрана/MGN-3 на компоненты клеток крови, функции печени и почек. Результаты показали, что Биобран/MGN-3 не оказывает влияния на общий процент NK-клеток, однако он усиливает цитотоксическую активность индуцированной NK-клетками экспрессии кластера дифференцировки 107а по сравнению с исходными значениями и контрольной группой (Р˂0,05). Кроме того, не было выявлено никаких побочных эффектов, что указывает на безопасность добавки Биобран/MGN-3 при используемых дозах и продолжительности применения. Наблюдались различные дополнительные благотворные влияния, включая улучшенный средний показатель гематокрита и уменьшенные уровни печеночного энзима – аспартатаминотрансферазы, что предполагает улучшение функции печени. Сделан вывод о том, что Биобран/MGN-3 индуцирует значительное повышение активности NK, что может повышать устойчивость к вирусным инфекциям и онкологическим заболеваниям в гериатрической популяции. Но для подтверждения этих выводов необходимо проведение дополнительных клинических испытаний.
Введение
Иммунодефицит в гериатрической популяции играет главную роль в повышенной восприимчивости пожилых людей к инфекциям, раку и нейродегенеративным заболеваниям. В процессе недавних исследований были найдены доказательства предположений, что ослабление нервной и иммунной системы тесно связаны между собой и с сохранностью гомеостаза. Несколько белков, первоначально считавшихся эксклюзивными для иммунной системы, обнаружили в здоровой нервной системе (4), а термин synaptoimmunology был недавно использован для характеристики взаимодействия между иммунными модуляторами и синаптической функцией (5). Связь между снижением иммунологической активности и увеличением инфекционных и раковых заболеваний обоснована результатами многочисленных исследований, которые показывают снижение качества лейкоцитарных функций при старении (6-9). Особый интерес для изучения иммунодефицита в гериатрической популяции представляют сообщения о возраст-зависимом уменьшении клеток натуральных киллеров (NK), которые составляют первую линию обороны в борьбе против злокачественных и вирус-инфицированных клеток (10-13). Поэтому повышение активности NK клеток в гериатрической популяции – важная терапевтическая цель.
Учитывая упомянутые выше значительные издержки, необходимо постараться найти естественные, безопасные и недорогие агенты для улучшения связанного с возрастом общего ухудшения здоровья и лечения заболеваний. Настоящее предварительное исследование мы построили на предположении, что полученная из рисовых отрубей натуральная пищевая добавка арабиноксилан ( Биобран / MGN-3) может противодействовать вызванному возрастными изменениями спаду активности NK-клеток у гериатрических пациентов старше 56 лет.
Биобран / MGN-3 изготовлен путем гидролиза рисовых отрубей с ферментным экстрактом грибов Шиитаке (14), и несколько исследований продемонстрировали его мощный иммуномодулирующий эффект (15-20). Например, было показано, что Биобран /MGN-3 в 2-3 раза повышает активность NK-клеток у молодых людей (испытуемых в возрасте 20-46 лет) (21). Эффект был дозо- и время-зависимым, и был связан с увеличением способности NK-клеток связываться с мишенями опухолевых клеток (21). Кроме того, положительный эффект Биобрана/MGN-3 на митогенный ответ T и B-клеток также был исследован in-vivo (14). Чтобы проверить нашу гипотезу, мы провели в течение месяца рандомизированное, двойное слепое, плацебо-контролируемое клиническое испытание у престарелых граждан, посещающих университетскую больницу Загазига в городе Загазиг Аль-Шаркия, Египет. Целью нашего исследования была оценка реакции этих престарелых граждан на иммуномодулирующее действие Биобрана / MGN-3 и определение возможности распространения положительного влияния Биобрана / MGN-3 на активность NK-клеток, о котором сообщалось ранее, на эту группу населения.
Темы и методы
Биобран/MGN-3 представляет собой денатурированную гемицеллюлозу, полученную при реакции гемицеллюлозы из рисовых отрубей с несколькими гидролизующими углеводы ферментами грибов Шиитаке. Это арабиноксилан с ксилозой в его главной цепи и полимером арабинозы в боковой (14). 500 мг Биобрана / MGN-3 испытуемые принимали внутрь один раз в сутки в виде порошка, расфасованного в пакетики (саше). Контрольная группа принимала такое же количество порошка плацебо, который был неотличим от Биобрана / MGN-3 по цвету, запаху и консистенции. Саше с Биобраном / MGN-3 и плацебо ничем не различались за исключением буквенного кода, отпечатанного на дне пакетика. И Биобран / MGN-3, и саше с плацебо были любезно предоставлены Daiwa Pharmaceuticals Co., Лимитед., Токио, Япония.
Состав материалов для исследования. Биобран/MGN-3 , расфасованный в пакетики, содержащие Биобран/MGN-3 (500 мг), Мальтит (1000 мг) Декстрин (200 мг), оксипропилированный дикрахмалфосфат (280 мг) и трикальцийфосфат (20 мг). В саше с плацебо содержится Мальтитол (1000 мг), Декстрин (200 мг), оксипропилированный дикрахмалфосфат (780 мг) и трикальцийфосфат (20 мг).
Критерии включения/исключения пациентов
Критерии включения. В исследование были включены субъекты в возрасте 56 лет и старше, готовые дать письменное согласие на добровольное участие.
Критерии исключения. Мы исключили пациентов с инфекциями или злокачественными новообразованиями, имеющимися в настоящее время или присутствующими в анамнезе, аутоиммунными расстройствами, выраженной портальной гипертензией и панцитопенией или серьезной психологической травмой. Мы также исключили тех, кто использовал витаминные или антибиотические добавки, женщин, которые кормили грудью, и пациентов, получавших противовирусное или противоопухолевое лечение (радиация, химиотерапия).
Субъекты и цели исследования. Двенадцать предположительно здоровых гериатрических испытуемых (≥56 лет) обоих полов (6 мужчин и 6 женщин) были случайным образом отобраны из посетителей поликлиник Университетской Больницы Загазига, Загазиг, Египет. Субъекты были рандомизированы либо в группу Биобран / MGN-3 (n=6, 500 мг / сут, перорально) либо в контрольную группу плацебо (n =6, 500 мг/сут, перорально) с использованием функции случайной выборки SPSS. Только у главного исследователя (ГИ) был код для группы Биобрана / MGN-3 и группы плацебо. Каждый участник сдал по 2 образца крови (по 4 мл) перед началом и окончанием исследования для лабораторных анализов и проточной цитометрии. Во время исследования испытуемых просили не брать без рецепта препараты, в том числе витамины, без консультации с главным исследователем.
Всех участников попросили сообщать о любых всплесках аномальных симптомов или признаков главному исследователю. Протокол исследования соответствовал этическим принципам Хельсинкской декларации 1975 года и был одобрен Советом по Институциональному обзору (одобрение IRB № 1507, июнь 2015), Университетская больница Загазиг, медицинский факультет.
Лабораторные анализы. Анализировалось количество клеток красной крови (эритроцитов,RBK), гематокрит (HCT), гемоглобин (Hb), средний корпускулярный гемоглобин (MCH), средний объем эритроцитов (MCV), количество тромбоцитов, клетки белой крови (лейкоциты), нейтрофилы и базофилы + эозинофилы.
В лабораторные исследования функции печени и почек были включен анализ аланинаминотрансферазы (сыровоточная глютамат-пируват трансаминаза) (ALT/SGPT), аспартатаминотрансфераза (сывороточная глутамат оксалоацетат трансаминаза) (АСТ/ SGOT) и мочевая кислота (UA). АЛТ, АСТ, ЩФ (ALP, щелочная фосфатаза) и уровень UA измерялись с помощью фотометрических методов с использованием анализатора COBAS Integra 400 plus (Roche, Базель, Швейцария).
Анализ на дегрануляцию. Кровь распределялась в объеме по 100 мкл в каждый из 4 капилляров для использования в качестве простимулированного и нестимулированного контроля, положительного контроля или отрицательного изотипического контроля IgG. Стимуляция NK/NKT клеток была проведена химически путем инкубации (5 ч, 37 ° С, менее 5% (v/v) CO2) в комбинации с форбол-12-миристат-13-ацетатом (РМА, 50 нг/мл; Сигма-Алдрич; Merck KGaA, Дармштадт, Германия) и Са2+ ионофором (Иономицином, 250 нг/мл, Сигма) в конечном объеме 500 мкл (с использованием среды RPMI-1640). Нестимулированные образцы инкубировали со средой RPMI-1640 без стимуляции РМА / Иономицином, тогда как в позитивные контрольные образцы цитохалазин (Sigma-Aldrich; Merck KGaA) добавляли совместно с РМА/Иономицином. FITC-меченый мышиный анти-человеческий CD-107a клон H4A3 (BD Bioscience, Сан-Хосе, Калифорния, США) был добавлен во время стимулирования PMA/Иономицином. Монензин (GolgiStop; BD Bioscience, San Jose, CA, USA) добавляли до конечной концентрации 6 мкг/мл через 1 ч после инкубации для блокирования интернализации и деградации CD107a. В пробирку с изотипическим отрицательным контролем IgG вместо CD107a (22) добавляли мышиный анти-человеческий FITC-меченный IgG AB (клон G18-145, BD Bioscience). После инкубации эритроциты лизировали BD PharmLyse (BD Bioscience) перед тем, как клетки были собраны путем центрифугирования, один раз промывали окрашивающим буфером и снова суспендировали в 100 мкл окрашивающего буфера. Клетки окрашивали путем инкубации с 5 мкл PE-меченого мышиного анти-человеческого CD56 AB клона R19-760 (NCAM-1, BD Bioscience) и 5 мкл меченого PerCP мышиного CD3-клона SK7 (BD Bioscience) в течение 15 мин при 37 ° С. Затем их собирали с помощью центрифугирования, промывали один раз FACS-буфером и повторно суспендировали в FACS-буфере. Анализ проводили с использованием BD FACSCalibur с программным обеспечением CellQuest (BD Bioscience).
Размер выборки. С помощью программного комплекса G*Power (Версия 3.1.9.2; Franz Faul, Германия) был выполнен анализ мощности выборки с использованием больших выборок 0,80 для повторного анализа дисперсии измерений с двумя измерениями в 2 группах. С критерием значимости (α), установленным на уровне 0,05, размер выборки из 6 субъектов в группе (всего 12 субъектов) в результате дал мощность 0,82 для получения статистически значимого результата.
Статистический анализ. Непрерывные переменные выражались в виде среднего ± стандартное отклонение. Для сравнения между группами использовали двусторонний t-критерий Стьюдента или точный критерий Фишера, в то время как для изучения эффективности лечения в группе использовали двусторонний парный t-критерий (т. е. сравнивали уровень после лечения с уровнем до лечения). Мы использовали тест Шапиро-Уилкса, чтобы определить, были ли данные нормально распределены. Для ненормально распределенных данных мы использовали непараметрический тест, ранговый критерий Уилкоксона и критерий Манна-Уитни для изучения эффективности лечения внутри и между группами соответственно. Статистически значимой разницей считали значение р ˂ 0,05. Для построения графиков использовался средний доверительный интервал ± 95%. Для анализа были использованы программа SPSS версии 22 (Корпорация IBM, Армонке, Нью-Йорк, США) и программа GraphPad Prism 6 (программное обеспечение программ GraphPad, Инк., La Jolla, CA, USA).
Результаты гематологического и биохимического профиля. Различные исходные параметры крови, энзимы печени и почечная функция были исследованы у 12 гериатрических субъектов как в группе Биобран/MGN-3 , так и в группе плацебо. Данные таблиц I и II показывают, что статистически значимых различий между двумя группами (р > 0,05) по всем исходным переменным, за исключением уровня АСТ (Р=0,041), не выявлено. Таблица I далее показывает, что не было существенной разницы между исходными значениями и значениями после 1 месяца приема добавки для измеренных характеристик в группе Биобран/MGN-3 , за исключением уровней Hb, MCV, MCH и AST (р ˂ 0,05). Таблица II показывает, что не было существенной разницы между исходными значениями и значениями после 1 месяца приема добавок для измеренных характеристик в группе плацебо, за исключением уровней Hb и MCH (р ˂ 0,05). Это также подтверждается отсутствием каких-либо побочных эффектов в группе Biobran / MGN-3, что указывает на безопасность лечения при вышеуказанных дозировке и продолжительности. Вместо этого после одного месяца лечения в группе Biobran / MGN-3 наблюдались некоторые положительные эффекты, в группе плацебо – в меньшей степени. Среди них – улучшение уровней Hb, MCV и MCH по сравнению с предварительными значениями. Кроме того, прием Биобран / MGN 3 значительно снижает уровни АСТ (SGOT), что говорит об улучшении функций печени.
Процент лимфоцитов, NK и NKT клеток. Данные таблицы III показывают, что исходные значения (до начала лечения) процентного содержания лимфоцитов, NK и NKT-клеток достоверно не различались между группами Биобрана/MGN-3 и плацебо (р > 0,05). Кроме того, в таблице III показано, что прием Биобрана/MGN-3 и плацебо в течение 1 месяца не вызывал значительных изменений в проценте лимфоцитов, клеток NK и NKT по сравнению с их исходными значениями (р > 0,05). Наблюдаемое увеличение % лимфоцитов находится в пределах нормы у взрослых и пожилых людей (18-44%).
NK-клетки, экспрессирующие CD107a. Для изучения влияния Биобрана / MGN-3 на дегрануляцию CD107a в активированных РМА / Иономицин NK-клетках проводили проточный цитометрический анализ. Добавка Биобран / MGN‑3 значительно усиливала стимулирование индуцированных РМА/Иономицином CD107a-экспрессирующих НК-клеток (Рис.Таблица IV). В обеих группах были выявлены аналогичные изменения уровня экспрессии CD107a в стимулированных PMA / Иономицином NK-клетках до начала лечения. Важно отметить, что сравнение процентных уровней предварительной обработки активированных PMA / Ионимицином NK-клеток, которые экспрессируют CD107a в группе Биобран / MGN 3 (60,5%) и группе плацебо (40,9%) (таблица IV), не проводилось с использованием теста Mann-Whitney U (результаты теста не показаны). Кроме того, на рис.2 показано влияние добавки Биобран / MGN-3 на повышение активности стимулированных NK-клеток, экспрессирующих CD107a,. Количество стимулированных PMA / Иономицином NK-клеток, которые экспрессируют CD107a, было значительно выше, чем исходные значения. С другой стороны, добавка для группы плацебо не повышала активность PMA / Иономицин-стимулированных NK, экспрессирующих CD107a. CD107a-позитивными было только очень небольшое число NK-клеток у пациентов с плацебо (рис.2). Данные исследования свидетельствуют о том, что добавление Биобрана / MGN-3 индуцирует экспрессию NK-клетками CD107a, параллельно с которой увеличивается цитотоксическое действие NK-клеток.
NKT клетки, экспрессирующие CD107a. Прием Биобрана / MGN-3 и плацебо незначительно усиливает процент стимулированных РМА/Иономицином NKT (CD3+ve, CD56+ve) клеток, экспрессирующих CD107a по сравнению с их исходными значениями
(Рис. 3 и Таблица IV).
Обсуждение
Биобран / MGN-3 – это арабиноксилан, полученный из рисовых отрубей. Он имеет ксилозу в своей основной цепи и полимер арабинозы в боковой (14). Биобран / MGN-3 является мощным модификатором биологического ответа (BRM), проявляемым способностью повышать активность NK-клеток и продуцирование IFN-γ лимфоцитами периферической крови in vitro (15), повышать активность NK у молодых взрослых людей (21) и больных раком (19,23,24). Биобран / MGN-3 также усиливает активность NK у животных, включая старых мышей (25) и животных-носителей опухолей. (17, 26). Это увеличение активности было связано с грануляцией NK-клеток и их способности связываться с мишенями опухолевых клеток (21,25,27). Дальнейшие исследования функции NK у гериатрических субъектов необходимы для выяснения преимуществ этого BRM у пожилых людей. NK-клетки представляют собой первую линию защиты от рака и инфицированных вирусами клеток вследствие того, что их цитотоксическая активность непосредственно убивает клетки-мишени. Однако нарушение активности NK из-за старения отмечается как у подопытных животных, так и у людей, и делает гериатрическую популяцию более восприимчивой к вирусным инфекциям и злокачественным новообразованиям (9,28-32).
ELSAID с соавт.: Биобран/MGN-3 активирует активность NK-клеток у ГЕРИАТРИЧЕСКИХ субъектов
Таблица I. Гематологические и биохимические характеристики (показатели крови, ферменты печени, функция почек) гериатрических больных в группе Биобран/MGN-3
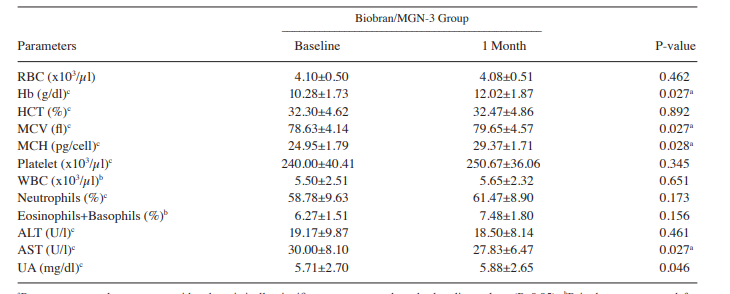
a)Значения после лечения считали статистически значимыми по сравнению с исходными значениями (р ˂ 0,05). b) Для нормально распределенных данных использовался парный t-критерий. c) Подтвержденный критерий ранжирования Уилкоксона для связанных образцов использовался для нерегулируемых распределенных данных. РБК, эритроциты; Hb, гемоглобин; HCT, гематокрит; MCV, средний объем эритроцитов; MCH, средний корпускулярный гемоглобин; WBC, лейкоциты; ALT, аланинаминотрансфераза; АСТ, аспартатаминотрансфераза; UA, мочевая кислота.
Таблица II. Гематологические и биохимические характеристики (параметры крови, энзимы печени, и почечная функция) гериатрических пациентов в группе плацебо.
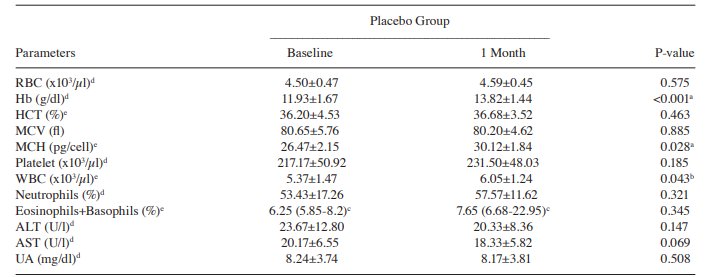
* Значения после лечения считали статистически значимыми по сравнению с исходными значениями (р ˂ 0,05). b) наблюдаемое увеличение % WBC в группе плацебо находится в пределах нормы у взрослых и пожилых людей и поэтому считалось незначительным (18-44%). c) Представлены медиана и IQR. d) Для нормально распределенных данных использовался парный t-критерий. e) Для ненормально распределенных данных использовался знаковый ранговый критерий Уилкоксона. RBC, эритроциты; Hb, гемоглобин; HCT, гематокрит; MCV, средний объем эритроцита; MCH, средний корпускулярный гемоглобин; WBC, лейкоциты; ALT, аланинаминотрансфераза; АСТ, аспартатаминотрансфераза; UA, мочевая кислота.
Возрастное снижение активности NK связано с уменьшением литического действия на клетку (31,32) и снижением экспрессии гранулированных перфоринов, которые в первую очередь ответственны за уничтожение рака и инфицированных вирусами клеток, что характерно как для NK-клеток, так и для цитотоксических T-лимфоцитов (32). Предварительные данные в этом исследовании показывают, что ежедневное употребление добавки Биобран / MGN-3 в дозе 500 мг / день в течение 1 месяца увеличивает активность NK-клеток в гериатрической популяции. Основной механизм неизвестен, но может быть связан с увеличением NK-гранулярных перфоринов и гранзимов-B (25,27) или со способностью Биобрана / MGN 3 влиять на ранние сигнальные события, приводящие к инициации протеинкиназы C (30).
ЭКСПЕРИМЕНТАЛЬНАЯ И ТЕРАПЕВТИЧЕСКАЯ МЕДИЦИНА 15: 2313-2320, 2018
Таблица III. Влияние Биобрана / MGN-3 и добавки-плацебо на процентлимфоцитов, NK и NKT внутри каждой группы перед лечением и после лечения.
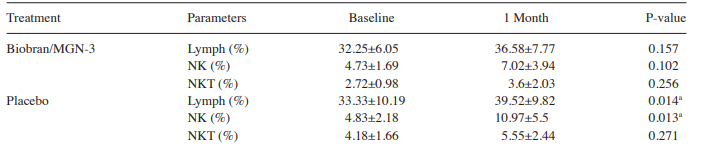
a) Наблюдаемое увеличение количества лимфоцитов и% NK-клеток в группе плацебо находится в пределах нормы у взрослых и пожилых людей, и поэтому считается клинически незначимым (18-44 и 7-28% соответственно). Для расчета значений P использовался двухсторонний парный t-критерий. NK, натуральные киллеры; NKT, натуральные Т-киллеры.
Таблица IV. Сравнение экспрессии CD107a на активированных клетках NK и NKT в каждой группе до и после лечения.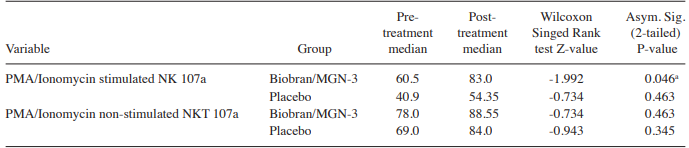
Значения после лечения считали статистически значимыми по сравнению со значениями до лечения (р ˂ 0,05). NK, натуральные киллеры; NKT, натуральные Т-киллеры ; Asym. Sig., асимптотические значения.
У лиц престарелого возраста в обеих группах (Биобран / MGN-3 и плацебо) были выявлены сходные незначительные изменения в уровнях экспрессии CD107a на NK-клетках, не содержащих PMA / Иономицина, в течение одного месяца после лечения по сравнению с исходными значениями. Однако добавление Биобрана / MGN 3 значительно повышало процентное содержание стимулированных PMA / Иономицином NK-клеток, экспрессирующих CD107a, по сравнению с исходным значением и группой плацебо (фиг.1). Повышенная регуляция Биобраном/ MGN-3 NK-экспрессии CD107a также хорошо иллюстрируется в проточной цитометрии, изображенной на рис.2B. У лиц из группы плацебо не наблюдалось активизации PMA / Иономицином рецепторов NK, экспрессирующих CD107a; CD107a-позитивными были лишь немногие NK-клетки (фиг.2A). Увеличение активности после лечения Биобраном / MGN-3 не было связано с процентным содержанием NK-клеток. Данные в таблице III показали, что существенных изменений в % лимфоцитов и % NK-клеток в группе Биобран / MGN 3 или плацебо не произошло. Эти данные соответствуют работам других исследователей, которые показывают, что нормальный диапазон лимфоцитов у здоровых людей составляет 18-44% (33), а нормальный диапазон NK-клеток составляет 7-28% (34,35). Сообщается, что экспрессия NK-клетками CD107a параллельна увеличению цитотоксического действия NK-клеток (22). Недавние исследования показали, что CD107a является не просто маркером дегрануляции, но играет ключевую роль в формировании лизосом и в процессе дегрануляции. RNAi-опосредованное молчание экспрессии CD107a в NK-клетках приводило к неспособности доставки гранзимов B к клеткам-мишеням, нарушению миграции перфорина, снижению содержания перфорина в литических гранулах и нарушенной цитотоксической активности NK-клеток (36).
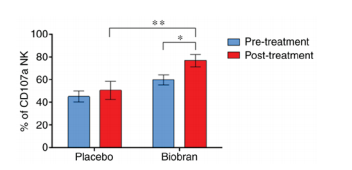
Рис. 1. Действие Биобрана/MGN-3 на процент химически активированных NK-клеток, которые экспрессируют CD107a. На фоне лечения добавкой Биобран/MGN-3 в течение 1 месяца значительно увеличился процент NK-клеток, экспрессирующих CD107a, которые были химически активированы PMA /Иономицином. Гистограмма представляет медианы ± IQR. Критерий ранжирования Уилкоксона и тест Манна-Уитни были использованы для сравнения внутри (до и после) и между группами (Биобран / MGN-3 и плацебо) соответственно. Не было обнаружено существенной разницы между уровнями предварительной обработки в двух группах. * Достоверно выше, чем PMA / Иономицин-стимулированные NK-клетки до лечения (P˂ 0,05). ** Достоверно выше, чем PMA / Иономицин-стимулированные NK-клетки при лечении группы плацебо (P˂ 0,05). NK, натуральный киллер.
С другой стороны, показано, что повышенная экспрессия CD107a коррелирует с секрецией цитокинов и цитотоксической активностью NK-клеток (37). Таким образом, наши результаты свидетельствуют о том, что добавка Биобран/MGN-3 увеличивает трафик литических гранул, дегрануляционную способность и цитотоксичность NK-клеток. NK-клетки считаются мостиком между врожденным ответом и адаптивной системой (38), и их активация приводит к модулированию других подмножеств иммунных клеток. Этот вывод был продемонстрирован в наших предыдущих исследованиях, которые показали способность Биобрана / MGN-3 модулировать человеческие CD8 + Т-клетки, CD4 + Т-клетки и В-клетки после приема внутрь (14).
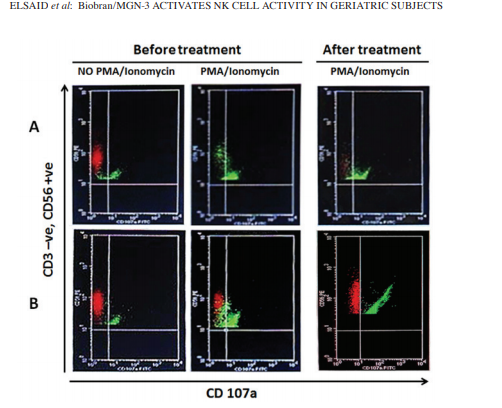
Рис. 2. Анализ проточной цитометрии, сравнивающий эффекты (A) плацебо и (B) добавки Биобран / MGN-3 на экспрессию CD107a в стимулированных PMA / Иономицином NK-клетках и не стимулированных PMA / Иономицином NK-клетках. Прием Биобрана / MGN 3 в течение 1 месяца значительно увеличивал количество CD107a-экспрессирующих NK-клеток при стимуляции PMA / Иономицином (справа внизу) по сравнению с клетками NK, стимулированными PMA / Иономицином перед добавлением Biobran / MGN-3 (нижняя средняя) и PMA / Иономицин-стимулированные NK-клетки после 1 месяца лечения плацебо (верхний правый). Уровни экспрессии CD107a в стимулированных PMA / Иономицином и нестимулированных PMA / Иономицином NK-клетках не были существенно различными в группах плацебо или Biobran / MGN 3 до лечения (средний и левый соответственно). NK, натуральный киллер.
Натуральные T-киллеры (NKT) являются разновидностью регуляторных лимфоцитов, которые со-экспрессируют рецепторы клеточной поверхности, характерные как для Т-лимфоцитов (например, CD3, α / β-Т-клеточные рецепторы [TCR]), так и для NK-клеток (например, CD56, NK1 .1) (39). Причина, по которой Биобран / MGN-3 индуцирует PMA / Иономицин-стимулированные NK-клетки, экспрессирующие CD107a, и не индуцирует NKT-клетки у гериатрических субъектов, не полностью понятна, но может быть отнесена к различиям в клеточных рецепторах NK-клеток и NKT-клеток. Проведенное нами ранее исследование показало, что добавление Биобрана / MGN-3 in vitro в течение 16 ч усиливает три основных рецептора клеточной поверхности на NK-клетках: CD69, антиген ранней активации; CD25, рецептор интерлейкина-2; и CD54 (ICAM-I), молекулу адгезии (15). NKT-клетки представляют собой популяцию Т-клеток, которые активируются липидными антигенами, связанными с молекулами CD1d (кластер дифференцировки 1d) на поверхности клеток, представляющих антиген. Существует пять различных CD1-генов (CD1a-e), которые были идентифицированы. CD1a-c белки распознаются различными традиционными αβ-Т-клетками, тогда как CD1d-белки распознаются специализированной разновидностью αβ -Т-клеток. Внутриклеточные метаболические пути липидных антигенов являются ключевыми в формировании функционального спектра клеток NKT (40,41). Мы полагаем, что для анализа их реакции на иммуномодулирующий эффект Биобрана / MGN-3 необходим детальный анализ липидной природы этих клеток.
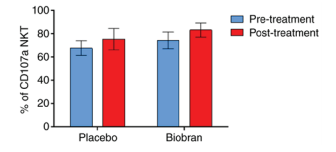
Рис. 3. Влияние Биобрана / MGN-3 на процент CD107a-экспрессирующих NKT (NKT-клеток), которые были химически стимулированы PMA / Иономицином. Добавка Биобран / MGN-3 не вызывала статистического значимого изменения процента CD107a-экспрессирующих NKT-клеток, которые были химически активированы с помощью PMA / Иономицином по сравнению с исходным уровнем или группой плацебо. Гистограмма представляет медианы ± IQR. Критерий Уилкоксона и тест Манна-Уитни были использованы для сравнения внутри (до и после) и между группами (Биобран / MGN-3 и плацебо) соответственно. NKT, натуральный Т-киллер.
Результаты данного исследования показали, что биологически активная добавка Биобран/MGN-3 усиливает активность NK-клеток у лиц пожилого возраста. Прямая связь между рационом и изменениями в структуре и деятельности мозга была описана в руководящих принципах Национального института ассоциации старения и болезни Альцгеймера. Рост экспериментальных данных свидетельствует о том, что синапсы могут быть локусом для аномалий, лежащих в основе таких заболеваний, как болезни Альцгеймера и Паркинсона, рассеянный склероз. Действительно, отклонения при индуцировании, поддержании или отмене долговременной потенциации синаптической передачи (LTP) и долгосрочной депрессии (LTD) являются общей нитью в различных моделях заболеваний головного мозга (42,43), а также в патологиях человека, связанных с воспалением (44). Таким образом, было высказано предположение, что этиопатогенез различных состояний является результатом сочетания аномальной экспрессии иммунных медиаторов с другими специфическими особенностями заболевания (5). Интересно отметить, что диетическая добавка L-триптофан предотвращает возраст-индуцированное снижение производства серотонина гиппокампа (5-НТ) и, таким образом, позволяет избежать когнитивного снижения (45), и что лечение силденафилом, ингибитором фосфодиэстеразы 5, привело к улучшению при синаптической дисфункции гиппокампа и дефиците памяти у мышиной модели болезни Альцгеймера (46). Результаты нашего исследования и результаты других исследований могут привести к разработке методов иммунонейрологической терапии.
Особенно интересно отметить, что NK-иммуномодулирующий эффект Биобрана/ MGN-3 у гериатрических испытуемых был достигнут при употреблении низкой дозы 500 мг / сут. Возрастные субъекты, которые участвовали в этом рандомизированном двойном слепом клиническом исследовании, были здоровыми, не жаловались на какие-либо заболевания и не принимали другие иммуномодуляторы, что указывало на выраженную реакцию здоровых возрастных субъектов на NK-иммуномодулирующий эффект Биобрана/ MGN- 3. Данные настоящего исследования показали, что Биобран / MGN-3 безопасен, и лечение им не вызывало каких-либо значительных токсических изменений в любом из проанализированных параметров. Напротив, после 1 месяца лечения в группе Биобран / MGN-3 наблюдались некоторые положительные эффекты, а в группе плацебо это проявлялось в меньшей степени. Эти эффекты включали улучшенные уровни Hb, MCH и ALP. Кроме того, добавка Биобран / MGN 3 значительно снижает уровни АСТ (SGOT), что говорит об улучшении функций печени. Это открытие согласуется с нашим недавним исследованием, которое показывает способность Биобрана / MGN-3 улучшать функции печени, о чем свидетельствует значительное снижение уровней виремии у пациентов с гепатитом C после лечения Биобраном / MGN-3 (47). Было показано, что Биобран / MGN-3 является безопасным и нетоксичным средством в нескольких исследованиях токсичности, включая: i) исследование субхронической токсичности у собак биглей, исследование антигенности морской свинки и испытание мутагенности (48,49); ii) LD50 (летальная доза, 50%) Biobran / MGN 3 превышает 36 г / кг; и iii) тест Эймса на мутагенность был отрицательным. Кроме того, исследования среди больных раком, получавших химиотерапию, показали значительное улучшение аппетита и других параметров качества жизни (QOL) (50,51).
Группа плацебо в этом исследовании принимала диетическое волокно, гидроксипропилдикарф фосфат (HDP), который в настоящее время используется в качестве пищевой добавки. Данные, представленные в таблицах II и III, показывают, что у субъектов, которые принимали HDP, выявлено значительное улучшение уровней Hb и MCH по сравнению с их исходными значениями. Более ранние исследования показали полезную роль пищевых волокон в общем состоянии здоровья. Например, субъекты, которые принимали HDP, показали значительно более низкую постпрандиальную реакцию глюкозы, инсулина и GIP, чем субъекты, которые принимали восковую кукурузную крахмальную муку (52). Кроме того, показано, что различные типы крахмала влияют на удержание 59Fe (53) и поглощение цинка и железа (54). Одним из ограничений нашего исследования было небольшое количество нашей выборки. Для подтверждения наших результатов необходимы исследования с выборками больших размеров. Другим ограничением была наша ограниченная способность изучать весь диапазон молекулярных маркеров, которые необходимы для выявления потенциальных механизмов, участвующих в активации Биобраном / MGN-3 NK, но не NKT-клеток.
В заключение, предварительные результаты этого исследования убедительно свидетельствуют о том, что Биобран / MGN-3, пищевая добавка из рисовых отрубей, может противодействовать иммуносенесценции NK-клеток у гериатрических пациентов, что указывает на потенциал Биобрана / MGN-3 для снижения заболеваемости раком и вирусных инфекций, характерных для пожилых людей. Насколько нам известно, настоящее исследование представляет собой первое клиническое испытание, которое расширяет действие модификатора биологического ответа (BRM) Биобрана / MGN 3, включающее усиление NK-клеток дегрануляционной и цитотоксической активности в гериатрической популяции. Биобран / MGN-3 является нетоксичным, недорогим дополнением и, таким образом, может служить средством снижения значительных затрат на здравоохранение, требующихся как здоровым, так и нездоровым гериатрическим субъектам. Наши дальнейшие направления исследований включают проведение многоцентровых перспективных клинических испытаний для оценки превентивной способности добавки Биобран / MGN-3 для снижения частоты инфекций и опухолевого генеза в гериатрической популяции.
Благодарности
Авторы хотели бы поблагодарить Daiwa Pharmaceutical Co., Ltd., Токио, Япония, за поставку Биобрана / MGN-3 для этого исследования. Это исследование частично поддерживалось грантами NIH-NIMHD. U54MD007598 и NIH / NCATS, а также грантами nos. UL1TR000124 и S21 MD000103. Авторы также хотели бы поблагодарить доктора Б. Дж. Виньюма из UCLA за помощь в написании рукописи и д-ра С. Голлапуди из UCI за обсуждения, связанные с экспериментальным дизайном и анализом.
06 Март 2015
06 Март 2015


